大伙儿应当都了解亲水性效用(hydrophobic effect),即溶液中非极性分子折叠式或质子化的状况,说实话便是,油与水不相溶。

亲水性效用说起来非常简单形象化,但它则是个心狠手辣!例如,在蛋清折叠式、药品-蛋清相互影响,及蛋清-蛋清相互影响中,亲水性效用经常是关键性原因之一呢[1]!
说到疏水性在药品-蛋清相互影响中的主要危害,实际上绝大多数发售的小分子药物都是有一定的疏水性[2]。试验也表明,亲水性相互影响对融合的奉献是十分极大的,可以做到约30 cal / (mol· ?)。这个是什么理念呢?例如,加上一个羟基(-CH3)造成的亲水性相互影响,对结合自由能的奉献是0.7kcal/mol,换句话说可以提高3.5倍上下的活力[1]!
亲水性相互影响这般广泛又这般关键,你是否会很好奇,它的实质究竟是什么?嗯,大家便是赏析这类追寻的精神实质!今日,我就和大家深扒一下亲水性相互影响,而且还会继续谈到二号主人公:去有机溶剂化(Desolvation)。
说到共价键或是离子键的实质,可以解释为电子云一定的程度的遍布相叠或是静电感应相互影响。可是,亲水性相互影响却没法从原子间的力来了解,例如你无法表述苯环上的一个碳原子到底是利用哪些原子间相互作用力勾引上羟基的碳原子,产生亲水性相互影响的。
那麼,推动亲水性相互影响的到底是何许人也呢?
说出来,实际上一点也不秘密,它便是“熵”(Entropic)[3]!我们知道在控温恒压管理体系下可以用吉布斯自由能(Gibbs Free Energy)分辨热学全过程是不是自发性,其方程式如下所示:
ΔG=ΔH?TΔS
这一方程式也来叙述物质的量浓度的融解全过程,当ΔG<0意味着融解全过程自发性,相反则并不是。表达式中ΔH指焓变,ΔS指的是熵变。
实际上这一方程式还可以用于叙述药品吸附和蛋清的相互影响全过程:一切的药品融合全过程实际上全是焓变和熵变的一同結果,仅仅我们在了解融合全过程时通常忽视了熵变的功效。
熵,是啥玩意儿呢?官方网界定,熵是管理体系下全部外部经济情况数的总数的当然对标值乘于玻尔兹曼常数。对这一界定不明白也没事儿,大家只必须了解,从活化能的视角,假如某类转变促使管理体系有越多的情况数,则有益于这类转变的自发性。
返回大家的吸水功效上,如果我们将疏水性的物质的量浓度扔进水里,那活化能怎样转变呢?最先水里原本的共价键互联网可能被毁坏以空出位置给疏水性物质的量浓度,这是一个吸热反应全过程。随后,在疏水性物质的量浓度周边,水分可能产生一个相近囚牢的构造,产生更为井然有序的共价键。
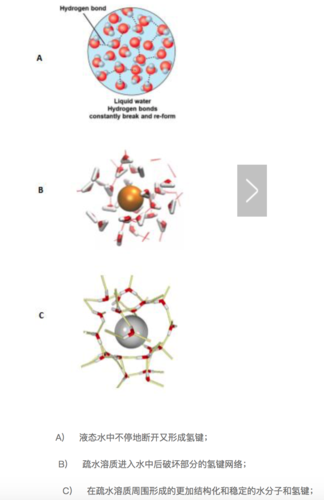
大家细想一下会发觉,整个过程中的焓变(ΔH)不好说是正、负或是相同的,由于新产生的共价键也许能赔偿第一步切断的共价键的动能。可是,疏水性物质的量浓度周边更为井然有序(结构型)的水分将促使管理体系的熵变(ΔS)减少,而且这一转变通常比焓变的转变更高。依据吉布斯自由能公式计算,ΔG=ΔH?TΔS,较小的ΔH(正负极不明)减掉一个负的比较大的ΔS,这一結果是正的,意味着着疏水性物质的量浓度没法自发性的融解到水里。当疏水性物质的量浓度集聚时,这一集聚的总体与水的了解表层比物质的量浓度彻底匀称分散化在饱和溶液中的了解面小,科学化的水分降至至少,随意的、有大量情况数的水分做到较多,与此同时熵也较大,这就是亲水性效用。

图中表明不一样环境温度下物质的量浓度融解的焓变、熵变和吉布斯自由能转变。横坐标意味着不一样溫度。下左图是LJ物质的量浓度融解到MB溶液中的基础理论预测分析結果,下图是亲水性物质的量浓度融解的研究結果。横坐标意味着溫度,能够看见不一样环境温度下疏水性物质的量浓度的融解吉布斯自由能全是正的,换句话说,不可以自发性融解。
返回小分子药物与蛋清相互影响管理体系上,如今有些人询问你,为何添加疏水性dna可以提升药品分子结构的活力呢?理解了如上所述的攻略大全,是不是你很简单地就能找到答案:由于疏水性官能团进到疏水性的蛋清袋子,促使产品的疏水性官能团尽量避免的泄露在溶液中,因此就使管理体系更为平稳进而提高活力。这一回应可以给100分吧?^_^
可是呢,还没完没了,假如我要告诉你,亲水性官能团与亲水基团的更换,乃至可以让活力转变4千倍,你是否会感觉难以想象?
来,不慌,大家再次聊~ 小故事或是得从亲水性效用谈起:在一些管理体系中,疏水性蛋清表层用一些适合的疏水性分子占有,大家发觉,这对结合自由能的奉献可以做到好多个kcal/mol [4]!例如下边这一事例:
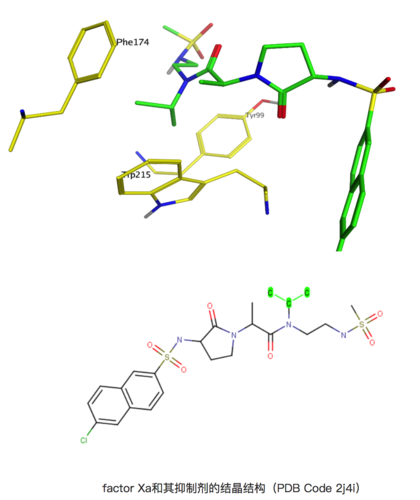
factor Xa和其缓聚剂的结晶体构造(PDB Code 2j4i)
图中是factor Xa和其缓聚剂(From GSK)的结晶体构造(PDB Code 2j4i),其Ki是1nM,可是假如将图例中高展示的异丙基换成氢(H),其活力立即降低到39μM,活力立即相距了4千倍!
图中事例中能够看见,Tyr99、Trp215和Phe174构成的疏水性的融合内腔,根据配位上的异丙基产生亲水性相互影响,进而提升活力。可是这一次,不提则已,一提便是令人震惊的4千倍!这是为什么呢?
说起清晰这个问题,就得请出今日的二号主人公,也是大伙儿在药品设计方案中非常容易忽视的,去有机溶剂化效用(desolvation)。
如下图清楚的叙述了该全过程,药品分子结构在溶液自然环境里进到靶点蛋清融合内腔的环节中,必须摆脱原先的水环境,而且将靶点融合袋子中的水排出来,这一环节中损耗或得到的动能便是去有机溶剂化能。
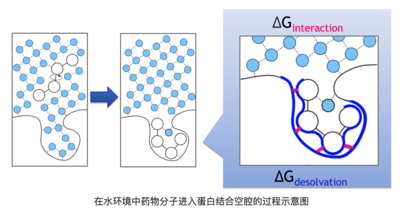
在水环境中药品分子结构进到蛋清融合内腔的全过程平面图
返回factor Xa的事例,我们在3D构造中看一下融合袋子的部位(下面的图),很显著,融合袋子并没有深层次蛋白內部,反而是在挨近有机溶剂所及的表层。假定沒有疏水性的异丙基占有,疏水性内腔部位很有可能占有着一些水分,一样这种在亲水性表层的水分会愈发的井然有序其情况数会较少,进而对结合自由能有不好的奉献;而根据异丙基可以协助排出来这种水分,进而得到除开亲水性相互影响外的一部分动能,因此活力被大大的增强了[5,6]。从这一事例中我们可以见到,药品设计方案中大家还要考虑到在无配位融合情况下融合袋子很有可能的水化情况!
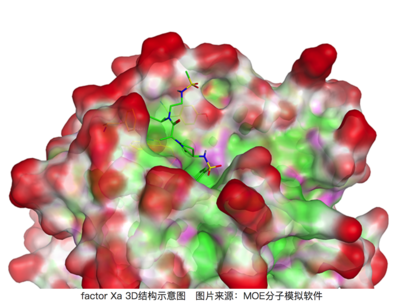
图中能够看见2j4i中的配位融合袋子在挨近蛋清表层,处在有机溶剂非常容易进到的地区。鲜红色部分意味着曝露有机溶剂中的地区,青绿色意味着亲水性地区,粉红色意味着正负极官能团地区。
特别注意的是,去有机溶剂化也是有将会会导致看上去可以有效地与蛋白激酶融合的分子结构实际上并无法有效地融合。例如在一个对于HIV-1蛋白酶抑制剂抗药性的探讨中发觉,由于基因突变造成融合袋子的去有机溶剂化能明显提升,进而致使了抗药性[7]。
再例如在有喹唑啉母环的化学物质是一类关键的EGFR(epidermal growth factor receptor,外皮转化成因素蛋白激酶)缓聚剂,吉非替尼和特罗凯都归属于该类药。例如下面的图的2个化学物质,下左图为知名药品特罗凯,下图为察觉的此外一个同系的EGFR缓聚剂(姑且称之为化学物质A)[8]。下图化学物质A能与EGFR 的Asp776产生离子键,大伙儿了解离子键能到达的键能是较强的,理论上,与特罗凯对比,化学物质A的活力提高应当远远不止10倍。
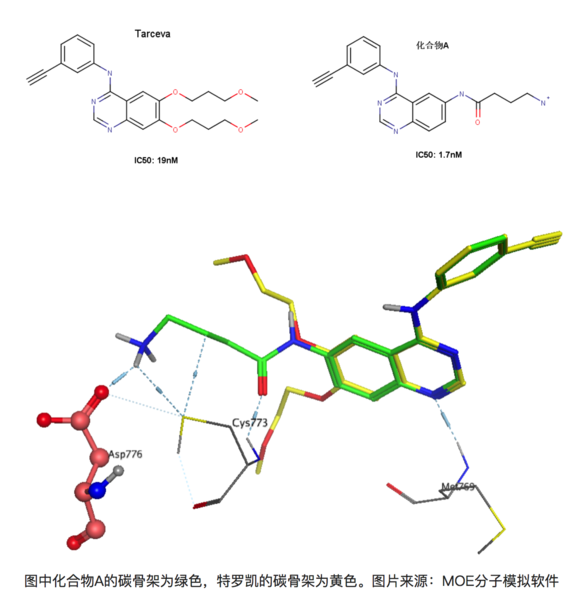
图中为化学物质A和特罗凯的叠合結果,能够看见化学物质A能和Asp776产生键能极强的离子键,可是活力却只提高了10倍!实际上这也是因为去有机溶剂化能的危害,Asp776坐落于有机溶剂所及的蛋清表层上,非常容易与水产生比较平稳的共价键,因而要与-NH3 功效时务必摆脱与一些水分的效果而消耗一定的动能。同样,化学物质A上的-NH3 也是一样的,必须断掉一部分与水产生的共价键取决于Asp776的羧基相互影响。因而看起来产生较强的共价键,可是因为去有机溶剂化的功效,其活力的增强不一定有想像中的理想化。
该文章内容提高散播新技术应用新闻资讯,很有可能有转截/引入之状况,若有侵权行为请联络删掉。
上一篇: 表面功能微纳结构及其加工方法介绍
下一篇: 木材外观自修复超疏水涂层的构建
 派旗纳米·官方网站
派旗纳米·官方网站
